භින්නෝන්මාදය හෙවත් schizophrenia යනු යොවුන්වියේදී ඇතිවිය හැකි මනෝව්යාධියකි. භින්නෝන්මාදයේ (Schizophrenia) පොදු රෝග ලක්ෂණ ප්රධාන කාණ්ඩ තුනකට බෙදිය හැකිය:
1. “ධනාත්මක” රෝග ලක්ෂණ (Positive Symptoms)
(මෙහි “ධනාත්මක” යනු සාමාන්ය අත්දැකීම්වලට යමක් එකතු වීමයි)
- මායා දර්ශන (Hallucinations): නොපවතින දේවල් අත්විඳීම. බහුලවම දක්නට ලැබෙන්නේ නොමැති කටහඬවල් ඇසීමයි. ඊට අමතරව නොපවතින දේවල් පෙනීමද සිදුවිය හැක.
- මුළාවන් (Delusions): සත්ය නොවන නමුත්, තර්ක කළ නොහැකි තරමට තදින් විශ්වාස කරන අදහස්. උදාහරණයක් ලෙස, අන් අය තමාට විරුද්ධව කුමන්ත්රණය කරන බව (පැරනොයාව), තමාට විශේෂ බලයක් ඇති බව, හෝ යමෙකු තමාගේ සිතුවිලි පාලනය කරන බව සිතීම.
- අවුල් සහගත චින්තනය සහ කථනය (Disorganized Thinking and Speech): සිතුවිලි එකිනෙක පැටලීම, අසම්බන්ධ ලෙස කතා කිරීම, එක් මාතෘකාවකින් තවත් මාතෘකාවකට ඉක්මනින් පැනීම, අන් අයට තේරුම් ගැනීමට අපහසු වීම.
2. “ඍණාත්මක” රෝග ලක්ෂණ (Negative Symptoms)
(මෙහි “ඍණාත්මක” යනු සාමාන්ය හැකියාවන් අඩු වීම හෝ නැති වී යාමයි)
- චිත්තවේගීය පැතලි බව (Emotional Flatness): මුහුණේ හැඟීම් ප්රකාශ නොවීම, කටහඬ ඒකාකාරී වීම (සතුටක්, දුකක් නොපෙන්වීම).
- අභිප්රේරණය නොමැතිකම (Avolition): එදිනෙදා වැඩකටයුතු (උදා: පිරිසිදුව සිටීම, ඉවුම් පිහුම් කිරීම) ආරම්භ කිරීමට හෝ කරගෙන යාමට උනන්දුවක් නොමැති වීම.
- සමාජයෙන් ඈත්වීම (Social Withdrawal): මිතුරන්ගෙන් සහ පවුලේ අයගෙන් ඈත්වීම, තනිව සිටීමට වැඩි කැමැත්තක් දැක්වීම.
- කතා කිරීම අඩු වීම (Alogia): කතා කිරීම ඉතාමත් අඩුවීම හෝ ප්රශ්නවලට ඉතා කෙටි පිළිතුරු දීම.
3. සංජානන රෝග ලක්ෂණ (Cognitive Symptoms)
(සිතීමේ ක්රියාවලියට අදාළ ගැටලු)
- අවධානය යොමු කිරීමේ අපහසුව: යම් දෙයක් කෙරෙහි අවධානය යොමු කිරීමට හෝ එය පවත්වා ගැනීමට ඇති අපහසුව.
- මතක ගැටලු: තොරතුරු මතක තබා ගැනීමට සහ අවශ්ය විටදී එය නැවත භාවිතා කිරීමට ඇති අපහසුව.
- තීරණ ගැනීමේ අපහසුව: තොරතුරු විශ්ලේෂණය කර තීරණයක් ගැනීමට නොහැකි වීම.
මෙම රෝග ලක්ෂණ පුද්ගලයාගෙන් පුද්ගලයාට වෙනස් විය හැකි අතර, රෝගයේ තත්ත්වය අනුව ඒවායේ බරපතලකමද වෙනස් විය හැක. ජානමය හේතු, මොළයට සිදුවන හානි, මව ගර්බිනී අවධියේ සිදුවූ වයිරස් ආසාදන, බාල අවධියේ අපයෝජනයට ලක්වීම සිට LSD, ඒක්ස්ටසි, ඇම්පිටමයින්, කංසා වැනි මත් ද්රව්ය භාවිතා කිරීම වැනි විවිධ හේතු නිසා භින්නෝනමාදය ඇතිවිය හැකි බව ශ්රී ලංකාවේ මානසික සෞඛ්යය පිළිබඳ ජාතික කවුන්සිලය පවසයි. පහත දැක්වෙන්නේ මෙම ව්යාධිය පිළිබඳ නවතම තොරතුරු අනාවරණය කරමින් සයන්ටිෆික් ඇමරිිිිකන් සඟරාවේ පළ වූ ලිපියකින් සකස් කළ විස්තරයකි.
ෂර්ලීන් සංකල්ට වයස අවුරුදු 19 දී, ඇයට අමුතු කටහඬවල් ඇසෙන්නටත්, විකාර සිතුවිලි ඇගේ මනස පුරවන්නටත් පටන් ගත්තේය. මිනිසුන්ට ඇගේ මනසට රිංගා ගැනීමට, ඇයට වස දීමට, ඇයව පොලිසියට පාවා දීමට අවශ්ය බව ඇයට සිතිණි. අන් අයට ඇගේ සිතුවිලි සොරකම් කළ හැකි යැයි විශ්වාස කළ ඇය, අන් අය දෙස කෙලින් බැලීම නතර කළාය. කලක් සමාජශීලී සහ පිටතට යනසුලු තැනැත්තියක වූ සංකල්, මිතුරන් සහ පවුලේ අය තමාට විරුද්ධව කුමන්ත්රණය කරන බවට කනස්සල්ලෙන්, ඔවුන්ගෙන් ඈත් වූවාය. රැකියාවට යන අතරමගදී, ඇගේ ඇස් කොනෙන් හිස් වැසුම් පැළඳි මිනිසුන්ගේ දර්ශන ඇය දුටුවාය. රෝගය උත්සන්න වෙත්ම, මිනිසුන් පවසන දේ තේරුම් ගැනීමේ හැකියාව ඇයට අහිමි වූ අතර, ඇය කතා කරන විට වචන නිවැරදිව පිට නොවීය. ඇගේ රෝග ලක්ෂණ ආරම්භ වී වසරකට පමණ පසු, සංකල්ට භින්නෝන්මාදය (schizophrenia) ඇති බව හඳුනා ගන්නා ලදී.
මුළාවන් (Delusions), මායා දර්ශන (hallucinations) සහ අවුල් සහගත චින්තනය සාමූහිකව මනෝව්යාධිය (psychosis) ලෙස හැඳින්වේ. මෙම “ධනාත්මක” (positive) රෝග ලක්ෂණ භින්නෝන්මාදයේ වඩාත් පුළුල් ලෙස පිළිගත් අංග අතර වේ. ලොව පුරා මිලියන 23 කට පමණ බලපාන භින්නෝන්මාද රෝගීන්ගෙන් තුනෙන් දෙකකට පමණ, සාම්ප්රදායික මනෝව්යාධි-විරෝධී ඖෂධ (antipsychotic drugs) මනෝව්යාධියට ප්රතිකාර කිරීම සඳහා බොහෝ විට ඉතා ඵලදායී වේ. නමුත් මෙම ඖෂධ බොහෝ විට ගැටලුකාරී අතුරු ආබාධ සමඟ පැමිණේ. තවද, චිත්තවේගීය පැතලි බව (emotional flatness) සහ සමාජයෙන් ඈත්වීම වැනි භින්නෝන්මාදයේ ඊනියා “ඍණාත්මක” (negative) රෝග ලක්ෂණ සඳහා හෝ සංජානන ගැටලු (cognitive problems) ලෙස හැඳින්වෙන චින්තනය සහ මතකය සම්බන්ධ වෙනත් ගැටලු සඳහා ඒවායින් ලැබෙන්නේ අඩු උපකාරයකි.
මෑතක් වන තුරුම, සියලුම මනෝව්යාධි-විරෝධී ඖෂධ ක්රියා කළේ අත්යවශ්යයෙන්ම එකම ආකාරයකටය. ඒවා මගින් ඩොපමයින් (dopamine) හි ක්රියාකාරිත්වය අවහිර කරන ලදී. ඩොපමයින් යනු අභිප්රේරණය, ඉගෙනීම, පුරුදු ගොඩනැගීම සහ වෙනත් ක්රියාවලීන් සඳහා සම්බන්ධ වන මොළයේ රසායනික පණිවිඩකරුවෙකි. ඩොපමයින් අවහිරක (dopamine blockers) මගින් මනෝව්යාධියට සාර්ථකව ප්රතිකාර කිරීම නිසා, භින්නෝන්මාදය තමන්ට වැටහෙන බවත්, එහි මූලික හේතුව ඩොපමයින් අසමතුලිතතාවයක් බවත් විශ්වාස කිරීමට බොහෝ වෛද්යවරුන් පෙළඹවීය. යම් රෝගියෙකුට යම් මනෝව්යාධි-විරෝධී ඖෂධයක් ක්රියා නොකළ විට, වෛද්යවරුන් සිතුවේ, ඔවුන් කළ යුත්තේ මාත්රාව වැඩි කිරීම හෝ ඩොපමයින් ඉලක්ක කරගත් වෙනත් ඖෂධයක් උත්සාහ කිරීම පමණක් බවයි.
නමුත් 2024 සැප්තැම්බර් මාසයේදී KarXT නම් නව ඖෂධයක පැමිණීම, භින්නෝන්මාදය ඔවුන්ගෙන් බොහෝ දෙනෙක් සිතුවාට වඩා සංකීර්ණ බවට වෛද්යවරුන් අතර මතුවෙමින් පවතින අවබෝධයට සහාය දක්වයි. KarXT යනු ඩොපමයින් හැර වෙනත් අණුවක් ඉලක්ක කළ පළමු මනෝව්යාධි-විරෝධී ඖෂධයයි. ඇතැම් පුද්ගලයින් තුළ ඩොපමයින් මෙම රෝගයේ ප්රධාන අංගයක් විය හැකි වුවද, එය මෙම රෝගයට සම්බන්ධ විවිධ ස්නායු සම්ප්රේෂකයන් (neurotransmitters) බොහොමයකින් එකක් පමණි. එම සංකීර්ණත්වය ප්රතිකාර සඳහා නව මංපෙත් විවර කර දිය හැකිය.
“භින්නෝන්මාදයක් කියා දෙයක් නැත. ඇත්තේ භින්නෝන්මාදයන් ය.” —රොමිනා මිස්රාහි, මනෝචිකිත්සාව පිළිබඳ මහාචාර්ය
මනෝව්යාධිය පිළිබඳ ජීවිත අත්දැකීම් ඇති, ඔක්ස්ෆර්ඩ් විශ්ව විද්යාලයේ ජ්යෙෂ්ඨ පර්යේෂකයෙකු වන තෝමස් කබීර්ට, KarXT හට මනෝව්යාධියේ රෝග ලක්ෂණ අඩු කිරීමට පමණක් නොව, චින්තනය වැඩි දියුණු කිරීමට ඇති හැකියාව විශේෂයෙන්ම උද්යෝගිමත් එකකි. “මිනිසුන්ට සාමාන්යයෙන් වසර ගණනාවක් තිස්සේ මායා දර්ශන සහ මුළාවන් ඇතිවන්නේ නැහැ,” ඔහු පවසයි. “මිනිසුන්ගේ එදිනෙදා ජීවිතයට ඇත්තෙන්ම බලපාන්නේ සංජානන ගැටලුයි.”
සමහරවිට වඩාත්ම වැදගත් දෙය නම්, භින්නෝන්මාදය මොළයේ පමණක් නොව ශරීරයේ ද – විශේෂයෙන් ප්රතිශක්තිකරණ පද්ධතියේ ද – වෙනස්කම් ඇතුළත් විය හැකි අතර, එය මෙම තත්ත්වය ඇති සෑම කෙනෙකු තුළම එකම ලෙස නොපෙනෙන බවට සාක්ෂි වර්ධනය වෙමින් පැවතීමයි. “භින්නෝන්මාදයක් කියා දෙයක් නැත. ඇත්තේ භින්නෝන්මාදයන් ය,” මැක්ගිල් විශ්ව විද්යාලයේ මනෝචිකිත්සාව පිළිබඳ මහාචාර්යවරියක වන රොමිනා මිස්රාහි පවසයි. වෛද්යවරුන්ට දැන් අවශ්යව ඇත්තේ, පුද්ගලයන් ඔවුන්ගේ රෝගයේ යටින් පවතින ජීව විද්යාව මත පදනම්ව වර්ගීකරණය කිරීමට ක්රමයක් බවත්, එවිට ප්රතිකාර ඔවුන්ගේ අවශ්යතාවලට වඩා හොඳින් ගැලපෙන පරිදි සකස් කළ හැකි බවත් ඇය වැඩිදුරටත් පවසයි.
ඉතිහාසය
සියවසකට වැඩි කාලයක් තිස්සේ විද්යාඥයින් භින්නෝන්මාදයේ ස්නායු-ජීව විද්යාත්මක පදනම තේරුම් ගැනීමට උත්සාහ කර ඇත. 1893 දී භින්නෝන්මාදයේ මුල්ම නිල විස්තරයක් ලියූ ජර්මානු මනෝ වෛද්ය එමිල් ක්රේප්ලින් (Emil Kraepelin) එය “dementia praecox” (අකල් ඩිමෙන්ශියාව) ලෙස හැඳින්වීය. මෙම තත්ත්වය නව යොවුන් වියේ හෝ තරුණ වැඩිහිටියන් තුළ පෙන්නුම් කිරීමට නැඹුරු වන නිසා, ක්රේප්ලින් කියා සිටියේ භින්නෝන්මාදය යනු බොහෝ විට වැඩිහිටියන්ට වැළඳෙන රෝගවලට සමාන ස්නායු-පරිහානීය (neurodegenerative) රෝගයක් බවයි.
ඊට වෙනස්ව, ස්විට්සර්ලන්ත මනෝ වෛද්ය ඉයුජන් බ්ලොයිලර් (Eugen Bleuler), සූරිච් හි රෙයිනාවු මනෝචිකිත්සක රෝහලේ රෝගීන් සමඟ ගත කළ දීර්ඝ වේලාවන් තුළ ඔවුන්ගේ හැසිරීම් පිළිබඳ දශකයකට වැඩි කාලයක් සූක්ෂම සටහන් තැබීය. ඔහු කියා සිටියේ මෙම රෝගය සැමවිටම ක්රමානුකූලව පිරිහීමක් හෝ නව යොවුන් වියේදී පමණක් ආරම්භ වීමක් නොවන බවයි. 1908 දී ඔහු “schizophrenia” (“භේද වූ මනස” යන අර්ථය) යන යෙදුම නිර්මාණය කළේ, මෙම තත්ත්වයේ කේන්ද්රීය ලෙස ඔහු දුටු මානසික ක්රියාකාරකම්වල ඛණ්ඩනය (fragmentation) සංලක්ෂිත කිරීමටය.
බ්ලොයිලර් වෙනත් ආකාරවලින් ද දුරදක්නා විය. ඔහු “භින්නෝන්මාද සමූහය” (the group of schizophrenias) ලෙස හැඳින්වූයේ, එය විවිධ බරපතලකම්, රෝග ලක්ෂණ වර්ණාවලියක් සහ විචල්ය ප්රතිඵල සහිත රෝග එකතුවක් (collection of disorders) බවට වූ ඔහුගේ දැක්ම පිළිබිඹු කරමිනි. තවද, මෙම රෝග සඳහා ජීව විද්යාත්මක මෙන්ම මනෝවිද්යාත්මක පදනමක් ද ඇති බව ඔහු උපකල්පනය කළේය. භින්නෝන්මාදය පවුල් තුළ දිව යාමේ ප්රවණතාවය එතැන් සිට ලේඛනගත කර ඇත – මෙම රෝගය 80% ක් පමණ පාරම්පරික වේ. නමුත් නිශ්චිත ජාන හඳුනා ගැනීම දුෂ්කර වී ඇති අතර, පර්යේෂකයන් සැක කරන්නේ ජාන සිය ගණනක් ඊට සම්බන්ධ විය හැකි බවයි. බොහෝ අධ්යයනයන් පරිසරයේ වැදගත්කම ද පෙන්වා දෙයි. ළමා වියේ අහිතකර අත්දැකීම්, ගර්භාෂය තුළ ආසාදනවලට නිරාවරණය වීම, නගරවල හැදී වැඩීම සහ අධික ලෙස ගංජා භාවිතය යන සියල්ල අවදානම වැඩි කිරීමට දායක වේ.
භින්නෝන්මාදය ළමා කාලයේ සිදුවන වෙනස්කම් තුළ මුල් බැස ඇති බවට සාක්ෂි වර්ධනය වුවද, භින්නෝන්මාදය ස්නායු-පරිහානීය රෝගයක් යන ක්රේප්ලින්ගේ අදහස තවමත් පවතී – එය දැඩි ලෙස විවාදයට ලක් වුවද. සමහර රෝගීන් තුළ, රෝග ලක්ෂණ කාලයත් සමඟ නරක අතට හැරෙන අතර, මෙම පිරිහීම බොහෝ විට මොළයේ පටක අහිමි වීම (tissue loss) සමඟ සිදු වේ. සමහර පර්යේෂකයන් තර්ක කර ඇත්තේ මෙම පිරිහීම ඒ වෙනුවට, දරිද්රතාවය සහ ආතතිය වැනි රෝගයට ද්විතියික සාධකවලට හේතු විය හැකි බවයි.
ඩොපමයින් අවහිරක
මනෝව්යාධි-විරෝධී ඖෂධ මුලින්ම මතු වූ විට, ඒවා මෙම චිත්රය බෙහෙවින් සරල කරන බවක් පෙනෙන්නට තිබුණි. 1950 ගණන්වලදී ප්රංශයේ මනෝ වෛද්යවරුන් දෙදෙනෙකු, ශල්යකර්ම සඳහා නිර්වින්දකයක් ලෙස නිර්මාණය කරන ලද සංයෝගයක් වන ක්ලෝර්ප්රොමසීන් (chlorpromazine), මායා දර්ශන සහ මුළාවන් සඳහා පිළියමක් බව අහම්බෙන් සොයා ගන්නා ලදී. ක්ලෝර්ප්රොමසීන් සහ ඉන් අනතුරුව ආ අනෙකුත් මනෝව්යාධි-විරෝධී ඖෂධ, ලොබොටොමි (lobotomies) වැනි භින්නෝන්මාදය සඳහා වූ බොළඳ සහ බොහෝ විට භයානක ප්රතිකාර යුගයක අවසානය ගෙන ආවේය.
මුලදී, ක්ලෝර්ප්රොමසීන් සහ එහි ව්යුත්පන්නයන් ක්රියා කළේ මන්දැයි කිසිවෙකු දැන සිටියේ නැත. පසුකාලීන මීයන් පිළිබඳ අධ්යයනයන්ගෙන් හෙළි වූයේ මෙම ඖෂධ ඩොපමයින් සඳහා වන ප්රතිග්රාහක (receptors) අවහිර කරන බවයි. (ප්රතිග්රාහක යනු කේත-අගුළු දැමූ දොරවල් ලෙස ක්රියා කරන අණු වන අතර, මෙම අවස්ථාවේ දී ඩොපමයින් වැනි ඇතැම් අණුවලට පමණක් සෛලයකට ඇතුළු වීමට ඉඩ සලසයි.) මෙම සොයාගැනීම්, ඩොපමයින් මුදා හරින බව දන්නා ඖෂධයක් වන ඇම්ෆෙටමින් (amphetamines) ඉහළ මාත්රාවලින් නිරෝගී පුද්ගලයින් තුළ කෙටිකාලීන මනෝව්යාධියක් ඇති කළ හැකි බවට නිරීක්ෂණ සමඟ එක්ව, භින්නෝන්මාදය පිළිබඳ ඊනියා ඩොපමයින් කල්පිතයට (dopamine hypothesis) මග පෑදීය. එයින් කියැවෙන්නේ භින්නෝන්මාදයේ රෝග ලක්ෂණ මොළයේ ඩොපමයින් අතිරික්තයක් නිසා ඇති වන බවයි.
මනෝව්යාධියට ප්රතිකාර කිරීමේදී ඵලදායී වුවද, ඩොපමයින් අවහිරක භින්නෝන්මාදය සඳහා දිව්යමය ඖෂධයක් (panacea) නොවේ. පාකින්සන් රෝගීන්ගේ (ඩොපමයින් හිඟකමෙන් පෙළෙන) වෙව්ලීමට සමාන වෙව්ලීම, නිදිමත ගතිය (sedation) සහ සැලකිය යුතු බර වැඩිවීමක් වැනි අතුරු ආබාධ රැසක් ඒවා සමඟ පැමිණේ, එමගින් දියවැඩියාව සහ හෘද රෝග ඇතිවීමේ අවදානම වැඩි කළ හැකිය. ඇත්ත වශයෙන්ම, ඩොපමයින් අවහිරක දිගු කලක් භාවිතා කළ ඉතිහාසයක් ඇති භින්නෝන්මාදයෙන් පෙළෙන පුද්ගලයින්ගේ මරණයට වඩාත් පොදු හේතුවක් වන්නේ හෘද වාහිනී රෝග (cardiovascular disease) ය.
ඇයගේ රෝග විනිශ්චයෙන් පසු වසරවලදී, සංකල් කිහිප වතාවක්ම රෝහල් ගත කරන ලද අතර, ඇයට දැඩි නොසන්සුන්කම, වෙව්ලීම සහ නිදිමත ගතිය ඇතුළු දරුණු අතුරු ආබාධ සහිත විවිධ ඖෂධ නියම කරන ලදී. එක් ඖෂධයක් කොතරම් දරුණු ලෙස ඇඟේ ඇඹරීම් (spasms) ඇති කළේද යත්, ඇයට චලනය වීමට හෝ කතා කිරීමට නොහැකි විය. ඖෂධ දෙකක් හෝ වැඩි ගණනකට පසුව රෝග ලක්ෂණ වැඩි දියුණු නොවන පුද්ගලයින්ට ලබා දෙන ලේබලයක් වන “ප්රතිකාර-ප්රතිරෝධී” (treatment-resistant) ලෙස සලකනු ලැබුවද, සංකල් අවසානයේ ඩොපමයින්-අවහිර කරන මනෝව්යාධි-විරෝධී ඖෂධයක් වන ක්ලෝසැපීන් (clozapine) සොයා ගත්තාය.
එහි අතුරු ආබාධ තිබියදීත්, එම ඖෂධය ඇගේ ජීවන තත්ත්වය සැලකිය යුතු ලෙස වැඩිදියුණු කිරීමට උපකාරී වී ඇති බව, දැන් 50 ගණන්වල පසුවන සහ දකුණු අප්රිකාවේ ‘ගෝලීය මානසික සෞඛ්ය සම ජාලයේ’ (Global Mental Health Peer Network) ප්රධාන විධායක නිලධාරී ලෙස සේවය කරන සංකල් පවසයි. නමුත් ප්රතිකාර-ප්රතිරෝධී භින්නෝන්මාදය ඇති පුද්ගලයින්ගෙන් 60% ක් දක්වා, ක්ලෝසැපීන් ද අකාර්යක්ෂම විය හැකිය.
ඩොපමයින් වලට වඩා වැඩි දෙයක්
දශක ගණනාවක් තිස්සේ ලබා ගත හැකි එකම මනෝව්යාධි-විරෝධී ඖෂධ වූයේ ඩොපමයින් අවහිරක පමණි. කෙසේ වෙතත්, 1990 ගණන්වල සිට, පර්යේෂකයන් පොසිට්රෝන-විමෝචන ටොමොග්රැෆි (PET) වැනි තාක්ෂණික ක්රම භාවිතා කිරීමට පටන් ගත්හ, එය ජීවමාන මොළය තුළ නිශ්චිත අණුවල ක්රියාකාරිත්වය බැලීමට ඉඩ සලසන රූපගත කිරීමේ ක්රමයකි. එම කාර්යය වඩාත් සංකීර්ණ කතාවක් යෝජනා කළේය.
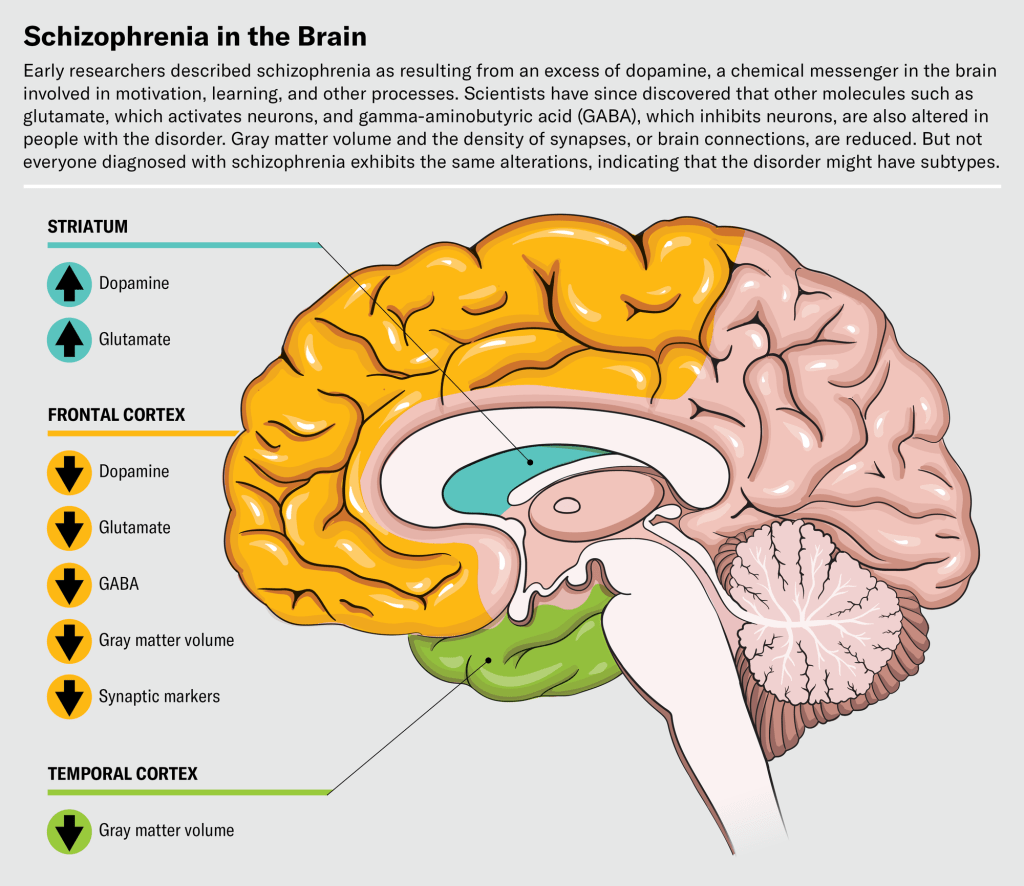
ස්නායු විද්යාඥයන් භින්නෝන්මාදය හා සම්බන්ධ මොළයේ ස්නායු රසායනික වෙනස්කම් හඳුනා ගැනීමට PET රූපගත කිරීම් සහ වෙනත් ක්රම භාවිතා කළහ. මොළයේ ගැඹුරින් පිහිටි ව්යුහයක් වන ස්ට්රයැටම් (striatum) හි නිශ්චිත කලාපයක ඩොපමයින් ක්රියාකාරිත්වය වැඩි වී ඇති බව ඔවුහු සොයා ගත්හ. ස්ට්රයැටම් ප්රධාන වශයෙන් සම්බන්ධ වන්නේ විෂම සිදුවීම් හෝ දේවල් අතර මානසික සම්බන්ධතා ගොඩනැගීමට අපට උපකාර කිරීම සඳහා ය. මෙම විෂමතාවය භින්නෝන්මාදය ඇති අයෙකු වැරදි ආශ්ර (false associations) හෝ වැරදි සංජානන (misperceptions) ඇති කර ගැනීමේ අවස්ථා වැඩි කළ හැකිය. ඊට අමතරව, විද්යාඥයන් සොයා ගත්තේ පූර්ව-ඉදිරිපස බාහිකයේ (prefrontal cortex) ඩොපමයින් මට්ටම අඩු වී ඇති බවත්, එමගින් ගැටලු විසඳීම සහ හැඟීම් නියාමනය කිරීම වැනි විධායක ක්රියාකාරකම්වලට (executive functions) බාධා කරන බවත්, එය මෙම තත්ත්වය ඇති පුද්ගලයින් තුළ අඩපණ විය හැකි බවත්ය.
මනෝව්යාධි-විරෝධී ඖෂධ සැමවිටම ක්රියා නොකරන්නේ මන්දැයි මෙම අධ්යයන මගින් ආලෝකයක් ලබා දෙන ලදී. 2012 දී, ලන්ඩනයේ කිංග්ස් කොලේජ් හි අණුක මනෝචිකිත්සාව පිළිබඳ මහාචාර්ය ඔලිවර් හවුස් (Oliver Howes) සහ ඔහුගේ කණ්ඩායම වාර්තා කළේ, සාම්ප්රදායික මනෝව්යාධි-විරෝධී ඖෂධවලට ප්රතිචාර නොදක්වන පුද්ගලයින්ගේ මොළයේ ඩොපමයින් ක්රියාකාරීත්වයේ රටා, ප්රතිචාර දක්වන අයට වඩා වෙනස් බවයි.
එවැනි විමර්ශන මගින් භින්නෝන්මාදයට සම්බන්ධ එකම ස්නායු සම්ප්රේෂකය ඩොපමයින් නොවන බව තහවුරු විය. අනෙක්වා අතරට ස්නායු සෛල සක්රීය කිරීමට සම්බන්ධ ප්රධාන අණුවක් වන ග්ලූටමේට් (glutamate) ඇතුළත් වේ. යේල් වෛද්ය විද්යාලයේ මනෝ වෛද්ය ජෝන් ක්රිස්ටල් (John Krystal) විසින් මෙහෙයවන ලද කණ්ඩායමක් මෙන්ම තවත් අය ද, ග්ලූටමේට් ක්රියාකාරිත්වය අවහිර කරන ඖෂධයක් වන කෙටමින් (ketamine) මගින් නිරෝගී පුද්ගලයින් තුළ මනෝව්යාධියේ රෝග ලක්ෂණ ඇති කළ හැකි බව පෙන්වා දී ඇත. භින්නෝන්මාදය හා සම්බන්ධ ජාන ප්රභේද සඳහා වන මහා පරිමාණ සෙවීම් මගින්, ග්ලූටමේට් සංඥාකරණයට (glutamate signaling) සම්බන්ධ ජානවල වෙනස්වීම්, මෙම රෝගය වර්ධනය වීමේ ප්රධාන අවදානම් සාධක අතර වන බව ද හෙළි වී තිබේ. මෑත දශක කිහිපය තුළ ග්ලූටමේට් ඉලක්ක කරගත් බොහෝ ඖෂධ නිපදවා ඇතත්, තවමත් කිසිවක් සායනික පරීක්ෂණ (clinical trials) හරහා සමත් වී නොමැත.
ඇසිටිල්කොලීන් (acetylcholine) නමැති තවත් ප්රධාන ස්නායු සම්ප්රේෂකයක්, ශරීරය සහ මොළය පුරා දක්නට ලැබෙන මස්කරිනික් ප්රතිග්රාහක (muscarinic receptors) මත ක්රියා කරයි. මේවා චලනය, මතකය සහ ඉගෙනීම වැනි ක්රියාවලීන් සඳහා සම්බන්ධ වේ. බ්රිස්ටල් මයර්ස් ස්ක්විබ් (BMS) විසින් කොබෙන්ෆි (Cobenfy) ලෙස අලෙවි කරනු ලබන නවතම භින්නෝන්මාද ඖෂධය වන KarXT, මොළයේ ඇති මස්කරිනික් ප්රතිග්රාහක තෝරා බේරා සක්රීය කරයි. සායනික පරීක්ෂණ වලදී, මෙම ඖෂධය මනෝව්යාධියට ප්රතිකාර කිරීමේදී ඵලදායී බව සොයා ගත් අතර, සාම්ප්රදායික මනෝව්යාධි-විරෝධී ඖෂධ රෝගීන්ට දිගු කාලයක් භාවිතා කිරීමට අපහසු වන අතුරු ආබාධවලින් තොරව, සංජානන ක්රියාකාරිත්වය වැඩි දියුණු කරන බවක් ද පෙනී ගියේය. මෙම ඖෂධයට ආමාශ ආන්ත්රික (gastrointestinal) බලපෑම් තිබූ අතර, ඉන් බොහොමයක් මෘදු ඒවා විය.
KarXT හි දිගුකාලීන බලපෑම් පිළිබඳ වැඩි දත්ත අවශ්ය වුවද, ඩොපමයින් සෘජුවම ඉලක්ක නොකරන එහි අද්විතීය ක්රියාකාරී යාන්ත්රණය හේතුවෙන්, භින්නෝන්මාද ක්ෂේත්රයේ පර්යේෂකයන් මෙම ඖෂධය පිළිබඳව උද්යෝගයට පත්ව සිටිති. කෙසේ වෙතත්, භින්නෝන්මාදයේ රෝග ලක්ෂණ සමනය කිරීමට මෙම ඖෂධය ක්රියා කරන්නේ කෙසේද යන්න තවමත් විවෘත ප්රශ්නයකි. මෙම යාන්ත්රණය සොයා ගැනීම, රෝගය පිළිබඳ අපගේ අවබෝධය සඳහා “ක්රීඩාව වෙනස් කරන්නෙකු” (game changer) විය හැකි බව හවුස් පවසයි. (හවුස්, BMS විසින් අත්පත් කර ගැනීමට පෙර ඖෂධය සොයා ගත් Karuna Therapeutics සඳහා උපදේශකයෙකු ලෙස සේවය කර ඇත.) “ඔබට සම්පූර්ණයෙන්ම නව ප්රතිග්රාහක කට්ටලයක් ඉලක්ක කර තවමත් කෙනෙකුට උපකාර කළ හැකි වීමෙන් අපට කියවෙන්නේ, භින්නෝන්මාදය සහ මනෝව්යාධිය පිළිබඳ අපගේ අවබෝධයේ යමක් අඩුවී ඇති බවයි,” කබීර් පවසයි.
ප්රතිශක්තිකරණ පද්ධතියේ සම්බන්ධය
භින්නෝන්මාදය හටගත හැකි තවත්, විශ්මයජනක ලෙස වෙනස් ආකාරයක් තිබේ. ඒප්රිල් බරල්, සියල්ල වෙනස් කළ කම්පන සහගත සිදුවීමක් වන තුරු, නිරෝගී, ජවසම්පන්න 21 හැවිරිදි තරුණියක වූවාය. ඇයට මනෝව්යාධිය සහ මායා දර්ශන ඇති වූ අතර, අවසානයේදී චලනය වීමට හෝ සන්නිවේදනය කිරීමට නොහැකිව සම්පූර්ණයෙන්ම චාලක-අක්රිය (catatonic) තත්වයකට පත් වූවාය. ඇයට භින්නෝන්මාදයේ දරුණු ස්වරූපයක් ඇති බව හඳුනා ගත් අතර, නිව් යෝර්ක් හි බ්රෙන්ට්වුඩ් හි පිල්ග්රිම් මනෝචිකිත්සක මධ්යස්ථානයට ඇතුළත් කරන ලද අතර, එහිදී ඇය වසර 20 කට ආසන්න කාලයක් ගත කළාය.
පිල්ග්රිම් හි මනෝ වෛද්යවරයකු වූ සැන්ඩර් මාක්ස් (Sander Markx) බහු-විශේෂඥ කණ්ඩායමක් එක්රැස් කර සම්පූර්ණ වෛද්ය පරීක්ෂණයක් ඇණවුම් කළ පසුවයි, බරල්ගේ වෛද්යවරුන් ඇගේ රුධිරයේ ස්වයං-ප්රතිදේහ (autoantibodies) අඩංගු බව සොයාගත්තේ – එනම්, ඇගේම ශරීරයට පහර දෙන, ඇගේ මොළයේ සෛල වලට හානි කරන ප්රතිදේහ. ඇයට ස්වයං ප්රතිශක්තිකරණ රෝගයක් (autoimmune disease) වන ‘ස්නායු-මනෝචිකිත්සක ලූපස්’ (neuropsychiatric lupus) ලෙස නව රෝග විනිශ්චයක් ලැබුණි. මාස හයක දැඩි ප්රතිශක්ති-මර්දන (immunosuppressive) ප්රතිකාර ක්රමයකින් පසු, බරල් 2020 දී සම්පූර්ණයෙන්ම පාහේ සුවය ලැබුවාය. “ඔබ සිතනු ඇත්තේ ඇය අලුත්ම පුද්ගලයෙක් කියායි,” ඇගේ සහෝදරයා වන ගයි බරල් 2023 දී වොෂින්ටන් පෝස්ට් පුවත්පතට පැවසීය.
ශරීරයේම ප්රතිශක්තිකරණ පද්ධතිය මොළයට පහර දෙන විට ඇතිවන රෝගයක් වන ස්වයං-ප්රතිශක්තිකරණ එන්සෙෆලයිටිස් (Autoimmune encephalitis) සොයාගනු ලැබුවේ දශක දෙකකටත් අඩු කාලයකට පෙරය. එය දැන ගැනීමට පෙර, මෙම රෝගයෙන් පෙළෙන බොහෝ දෙනෙකුට – බරල් මෙන්ම – තත්ත්වයන් දෙක අතර යම් සියුම් වෙනස්කම් තිබියදීත්, භින්නෝන්මාදය යන රෝග විනිශ්චය ලැබෙන්නට ඇත. උදාහරණයක් ලෙස, ස්වයං-ප්රතිශක්තිකරණ එන්සෙෆලයිටිස් ඇති පුද්ගලයින් තුළ, රෝග ලක්ෂණ වඩාත් වේගයෙන් දිස්වීමට සහ වඩාත් දරුණු වීමට නැඹුරු වේ.
ස්වයං-ප්රතිශක්තිකරණ එන්සෙෆලයිටිස් හි පළමු අවස්ථා කිහිපයක් 2007 දී වාර්තා විය. එවකට පෙන්සිල්වේනියා විශ්ව විද්යාලයේ ස්නායු විශේෂඥයෙකු වූ ජොසෙප් ඩල්මාවු (Josep Dalmau) සහ ඔහුගේ සගයන්, NMDA ප්රතිග්රාහකයට එරෙහිව ස්වයං-ප්රතිදේහ ඇති රෝගීන් පිළිබඳ විස්තර ප්රකාශයට පත් කළහ. NMDA ප්රතිග්රාහකය යනු භින්නෝන්මාදය ඇති පුද්ගලයින් තුළ වෙනස් වන ප්රධාන ස්නායු සම්ප්රේෂකයක් වන ග්ලූටමේට්, එහි ක්රියාව සිදු කරන මොළයේ ඇති ප්රෝටීනයයි. එතැන් සිට වසර ගණනාවක් පුරා, පර්යේෂකයන් මොළය ඉලක්ක කරන ස්වයං-ප්රතිදේහ දුසිම් දෙකකට වඩා ලේඛනගත කර ඇත. මොළය සහ සුෂුම්නාව හරහා ගලා යන ද්රවය වන මස්තිෂ්ක සුෂුම්නා තරලය (CSF) තුළ ස්වයං-ප්රතිදේහ හඳුනා ගැනීම බොහෝ විට අවශ්ය වන, ස්වයං-ප්රතිශක්තිකරණ එන්සෙෆලයිටිස් රෝග විනිශ්චය, ජීවිතය වෙනස් කරන්නක් විය හැකිය. ප්රතිශක්තිකරණ ප්රතිකාර (immunotherapy) ලබන සමහර රෝගීන් පූර්ණ සුවය ලබයි.
ස්වයං-ප්රතිශක්තිකරණ එන්සෙෆලයිටිස් හි පැහැදිලි අවස්ථා දුර්ලභ ය. සමහර ඇස්තමේන්තු වලට අනුව, මනෝව්යාධිය ඇති පුද්ගලයින්ගෙන් 1% කට පමණ මොළයේ නිශ්චිත ඉලක්කය හඳුනාගෙන ඇති ස්වයං-ප්රතිදේහ ඇත. නමුත් CSF ලබා ගැනීමට අවශ්ය වන කශේරුකා සිදුරු කිරීම (lumbar punctures), මනෝව්යාධිය ඇති බොහෝ අය ප්රතිකාර සඳහා යන මනෝචිකිත්සක සායනවලදී (psychiatry clinics) කලාතුරකින් සිදු කරන බැවින්, සැබෑ ව්යාප්තිය තීරණය කිරීම දුෂ්කර ය.
ජර්මනියේ ෆ්රයිබර්ග් විශ්ව විද්යාලයේ සහ ඊට අනුබද්ධ රෝහලේ, මනෝව්යාධිය ඇති පුද්ගලයින් සඳහා කශේරුකා සිදුරු කිරීම සාමාන්ය දෙයක් වන අතර, එහි සේවය කරන මනෝ වෛද්ය ලුඩ්ගර් ටෙබාර්ට්ස් වැන් එල්ස්ට් (Ludger Tebartz van Elst) ට අනුව, ඔහුගේ කණ්ඩායම මනෝව්යාධිය සහ අනෙකුත් මනෝචිකිත්සක තත්ත්වයන් ඇති රෝගීන්ගෙන් ආසන්න වශයෙන් 20% ක පමණ හඳුනා නොගත් ස්නායු ස්වයං-ප්රතිදේහ (uncharacterized neuronal autoantibodies) (එනම් මනෝව්යාධියට හේතු ලෙස පැහැදිලිව ස්ථාපිත කර නොමැති ස්වයං-ප්රතිදේහ) සොයාගෙන ඇත. ඒ අනුව, ටෙබාර්ට්ස් වැන් එල්ස්ට් සහ තවත් අය මෙම රෝගීන්ගේ රෝගාබාධ විස්තර කිරීම සඳහා “ස්වයං-ප්රතිශක්තිකරණ මනෝව්යාධිය” (autoimmune psychosis) යන යෙදුම භාවිතා කිරීමට පක්ෂව කතා කරති.
මෙම විශේෂිත නොවන ස්වයං-ප්රතිදේහ භින්නෝන්මාදය සහ අනෙකුත් මනෝව්යාධි ආබාධ සඳහා අර්ථවත් කාර්යභාරයක් ඉටු කරන්නේද යන ප්රශ්නය මෑත වසරවල දැඩි විවාදයට ලක් වූවකි. මනෝව්යාධිය ඇති පුද්ගලයින් තුළ ඒවායේ ව්යාප්තිය පිළිබඳ අධ්යයනයන් (බොහෝ විට CSF සැමවිටම ලබා ගත නොහැකි නිසා රුධිරය පරීක්ෂා කරයි) නොගැලපෙන ප්රතිඵල පෙන්වා ඇත. පර්යේෂකයන් මෙම ප්රතිදේහ නිරෝගී පුද්ගලයින් තුළ ද සොයාගෙන ඇති අතර, ඒවායේ සායනික වැදගත්කම පිළිබඳව සැක මතු කර තිබේ.
තවත් සමහරු විශ්වාස කරන්නේ ස්වයං-ප්රතිදේහ නොමැති විට පවා ප්රතිශක්තිකරණ පද්ධතිය මනෝව්යාධියට දායක විය හැකි බවයි. ඉන්ෆ්ලුවෙන්සා, සිපිලිේ සහ වඩාත් මෑතක දී COVID වැනි ආසාදන මගින් ඇති වූ මනෝව්යාධි අවස්ථා ඉතිහාසය පුරා විසිරී ඇත. ඊට අමතරව, වසංගත රෝග විද්යාත්මක අධ්යයනයන් වාර්තා කර ඇත්තේ, ගිම්හානයේදී උපත ලබන අයට සාපේක්ෂව, ආසාදන බහුලව පවතින ශීත ඍතුවේ දී උපත ලබන පුද්ගලයින් තුළ භින්නෝන්මාදය වැනි මානසික ආබාධ වැඩි සංඛ්යාවක් ඇති බවයි. ඩෙන්මාර්කය වැනි වෛද්ය දත්ත පිළිබඳ ජාතික ලේඛනාගාර තබා ගන්නා රටවල තක්සේරු කිරීම්වලින් හෙළි වී ඇත්තේ පුද්ගලයෙකුට ඇති ආසාදන සංඛ්යාව වැඩි වන තරමට භින්නෝන්මාදය වැළඳීමේ අවදානම ද වැඩි වන බවයි.
ආසාදන මගින් සෘජුවම මනෝව්යාධිය ඇති කළ හැකිද යන්න අවිනිශ්චිතව පැවතියද, වසර ගණනාවක් පුරා බොහෝ අධ්යයනයන් මගින් ප්රතිශක්තිකරණ පද්ධතිය වැරදිකරු බවට සාක්ෂි සපයා ඇත. භින්නෝන්මාදය ඇති පුද්ගලයින් පිළිබඳ ජානමය විමර්ශන මගින් ප්රතිශක්තිකරණ පද්ධතියට සම්බන්ධ ප්රධාන ප්රෝටීන හා සම්බන්ධ ජාන හඳුනාගෙන ඇත. තවද, මොළයේ නේවාසික ප්රතිශක්තිකරණ සෛල වන මයික්රොග්ලියා (microglia), භින්නෝන්මාදය ඇති පුද්ගලයින් තුළ අධි-ක්රියාකාරී වන අතර, සමහර විද්යාඥයින් ඒවා මෙම රෝගයට සම්බන්ධ බව යෝජනා කිරීමට පෙළඹී ඇත.
ගැලපෙන ප්රතිකාර සෙවීම
භින්නෝන්මාද රෝග විනිශ්චය ලබන පුද්ගලයින්ගෙන් වැඩි ප්රතිශතයකට ප්රතිශක්තිකරණ පද්ධතිය සම්බන්ධ විය හැකිද යන්න පර්යේෂකයෝ දැන් අධ්යයනය කරමින් සිටිති. සමහර කණ්ඩායම්, ස්වයං ප්රතිශක්තිකරණ රෝගයක් සඳහා වන නිර්ණායක සපුරාලන්නේ නැති, භින්නෝන්මාදය සහ අනෙකුත් මනෝව්යාධි-ආශ්රිත ආබාධ ඇති පුද්ගලයින්ට ප්රතිශක්තිකරණ ප්රතිකාර (immunotherapies) උපකාර කළ හැකිද යන්න විමර්ශනය කිරීම සඳහා සායනික පරීක්ෂණ පවත්වයි.
ඔක්ස්ෆර්ඩ්හිදී, කබීර්, මනෝචිකිත්සා මහාචාර්ය බෙලින්ඩා ලෙනොක්ස් (Belinda Lennox) සහ ඔවුන්ගේ සගයන්, ආතරයිටිස් සහ අනෙකුත් ස්වයං ප්රතිශක්තිකරණ ආබාධ සඳහා ප්රතිකාර කිරීමට භාවිතා කරන ප්රතිදේහයක් වන රිටුක්සිමාබ් (rituximab) මගින්, රුධිරයේ හඳුනාගත හැකි ස්නායු ස්වයං-ප්රතිදේහ ඇති පුද්ගලයින්ගේ මනෝව්යාධියට ඵලදායී ලෙස ප්රතිකාර කළ හැකිද යන්න පරීක්ෂා කිරීම සඳහා සායනික පරීක්ෂණයක් පවත්වයි. ස්වීඩනයේ උප්සලා විශ්ව විද්යාලයේ මනෝ වෛද්යවරියක වන ජැනට් කනිංහැම් (Janet Cunningham) සහ ඇගේ කණ්ඩායම ද එම රටේ ද එවැනිම අධ්යයනයක් සිදු කරයි. මෙම පුද්ගලයින්ගෙන් කුඩා ප්රතිශතයක් හෝ මෙම ප්රතිකාර සඳහා ප්රතිචාර දක්වන්නේ නම්, එය පරිවර්තනීය වනු ඇත, “මක්නිසාද යත් ඔබට ඔවුන්ගේ ජීවිත කාලය පුරාම පවතින රෝගය සුව කළ හැකි බැවිනි,” ලෙනොක්ස් පවසයි.
මනෝව්යාධිය සඳහා ප්රතිශක්තිකරණ ප්රතිකාර කිරීමේ හැකියාව පිළිබඳව බොහෝ උද්යෝගයක් පවතියි, නමුත් විශේෂඥයින් මෙම ආබාධයේ ප්රතිශක්තිකරණ පදනම මත පමණක් අවධානය යොමු කිරීමට එරෙහිව අනතුරු අඟවයි. රෝගීන්ට සමහර විට භින්නෝන්මාදයට වඩා “ස්වයං-ප්රතිශක්තිකරණ මනෝව්යාධිය” වඩාත් පිළිගත හැකි රෝග විනිශ්චයක් ලෙස දැකිය හැකිය, මන්ද එය සුවය ලැබීමට වඩාත් බලාපොරොත්තු සහගත මාර්ගයක් සැපයිය හැකි බැවිනි – තවද එය “භින්නෝන්මාදය” යන වචනය වටා ඇති களங்கයෙන් (stigma) වැළකී සිටීමට ඉඩ සලසන බැවිනි. නමුත් ප්රතිශක්තිකරණ ප්රතිකාර ද ඒවායේ අවදානම්වලින් තොර නොවේ. ස්වයං-ප්රතිශක්තිකරණ මනෝව්යාධි අවස්ථාවන්හිදී බොහෝ විට භාවිතා වන කෝටිසෝන් (cortisone) වැනි ඖෂධ, අස්ථි බිඳෙනසුලු බව, තුවාල සුවවීම ප්රමාද වීම සහ මනෝභාවය වෙනස් වීම සහ ව්යාකූලත්වය වැනි මනෝවිද්යාත්මක බලපෑම් ඇතුළු ඒවාටම ආවේණික අතුරු ආබාධ සමඟ පැමිණේ.
කනිංහැම් පවසන්නේ පවතින මනෝව්යාධි-විරෝධී ඖෂධ, භින්නෝන්මාදය සහ අනෙකුත් මනෝව්යාධි-ආශ්රිත ආබාධ ඇති බොහෝ දෙනෙකුට උපකාර වන බව මතක තබා ගැනීම වැදගත් බවයි. “අප සතුව ඇති ඖෂධවලින් බොහෝ දෙනෙකුට උපකාර ලැබෙන මට්ටමකට අපි පැමිණ තිබෙනවා,” ඇය පවසයි. “දැන් අපට උපකාර කිරීමට නොහැකි අය දෙස බැලිය යුතුයි.”
මනෝව්යාධිය පිළිබඳ ජීවිත අත්දැකීම් ඇති ඔක්ස්ෆර්ඩ් පර්යේෂක කබීර්, මුලින්ම රෝගාතුර වූයේ ඔහු විශ්ව විද්යාල ශිෂ්යයෙකුව සිටියදීය. ඔහුගේ ප්රමුඛතාවය වූයේ රෝහලෙන් පිටත සිටීම සහ ඔහුගේ උපාධිය සම්පූර්ණ කිරීමයි. එය කිරීමට ඇති වේගවත්ම ක්රමය වූයේ ඖෂධ ලබා ගැනීමයි. නමුත් පසුව, ඔහුගේ රෝග ලක්ෂණ ස්ථාවර වූ පසු, ඔහු කථන ප්රතිකාර (talk therapy) ද එක් කර ගත් අතර, එය මනෝව්යාධියේ රෝග ලක්ෂණ සහ මානසික අවපීඩනය වැනි වෙනත් ගැටලු සඳහා ද උපකාරී වූ බව ඔහු පවසයි. කබීර්ට අනුව, වර්තමාන ප්රතිකාරවල ඇති ලොකුම සීමාවක් නම්, ස්ත්රී-පුරුෂ භාවය, වයස හෝ රෝගයේ අවධිය වැනි සාධක මත පදනම්ව මිනිසුන්ට විවිධ ඖෂධ සහ විවිධ මාත්රා අවශ්ය විය හැකි බවට පර්යේෂණ යෝජනා කළද, මනෝව්යාධිය ඇති පුද්ගලයින්ට බොහෝ දුරට සමාන ලෙස – එකම ඖෂධ කට්ටල, බොහෝ විට සමාන මාත්රාවලින් – ප්රතිකාර ලැබීමයි.
සමහර විශේෂඥයන් පවසන්නේ, එක් එක් රෝගියා සඳහා වඩාත් ඵලදායී ප්රතිකාරය හඳුනා ගැනීම සඳහා, වෛද්යවරුන් විසින් රෝගයකට යටින් පවතින හේතුව තීරණය කිරීමට අවශ්ය විය හැකි බවයි. ටෙබාර්ට්ස් වැන් එල්ස්ට්ගේ ෆ්රයිබර්ග් හි සායනයේදී, මනෝව්යාධිය අත්විඳීමෙන් පසු පැමිණෙන රෝගීන්ට, රෝග ලක්ෂණ සඳහා ද්විතියික හේතුවක් බැහැර කිරීම සඳහා, ස්නායු රූපගත කිරීම් (neuroimaging), රුධිර පරීක්ෂණ සහ කශේරුකා සිදුරු කිරීමක් ඇතුළත් වන සම්පූර්ණ පරීක්ෂාවකට ලක් කෙරේ. කෙසේ වෙතත්, එවැනි පුළුල් පරීක්ෂණ සාමාන්ය දෙයක් නොවේ. එක්සත් ජනපදය ඇතුළු ලෝකයේ බොහෝ ප්රදේශවල, පුද්ගලයෙකුට මෙම වර්ගයේ පරීක්ෂණ ලැබේද නැද්ද යන්න බොහෝ දුරට රඳා පවතින්නේ ඔවුන් මනෝ වෛද්යවරයකුගේ හෝ ස්නායු විශේෂඥයකුගේ කාර්යාලයට පැමිණීම මතය.
භින්නෝන්මාදය ඇති පුද්ගලයින් වඩා හොඳින් සංලක්ෂිත කිරීමට උත්සාහ කරන විශාල, අඛණ්ඩ උත්සාහයන් කිහිපයක් තිබේ. MIT සහ හාවඩ් හි බ්රෝඩ් ආයතනයේ ස්ටීවන් ඊ. හයිමන් (Steven E. Hyman) විසින් මෙහෙයවනු ලබන ‘මනෝචිකිත්සක ජෛව සලකුණු ජාලය’ (Psychiatric Biomarker Network), මස්තිෂ්ක සුෂුම්නා තරලයේ ජෛව සලකුණු (biomarkers) සොයා ගැනීමේ අරමුණින් 2018 දී ස්ථාපිත කරන ලදී. 2020 දී එක්සත් ජනපදයේ සහ යුරෝපා සංගමයේ රාජ්ය සහ පෞද්ගලික ආයතන කිහිපයක් විසින් දියත් කරන ලද ‘Accelerating Medicines Partnership Schizophrenia’ හට ද සමාන අරමුණක් ඇත. රෝග ලක්ෂණ මතු වීමට පෙර කාල පරිච්ඡේදය වන භින්නෝන්මාදයේ “පූර්ව” (prodromal) අවධියේ සිටින පුද්ගලයින් හඳුනාගත හැකි සලකුණු සොයා ගැනීමට පර්යේෂකයෝ බලාපොරොත්තු වෙති.
මෙම අදියරේදී පුද්ගලයින් හඳුනා ගැනීමට හැකිවීම, “වැළැක්වීමේ ප්රතිකාර (preventive treatments) දියුණු කිරීමට උත්සාහ කිරීමේ හැකියාව විවෘත කරනු ඇත,” හවුස් පවසයි. ඔහුගේ කණ්ඩායම ස්නායු රූපගත කිරීමේ සලකුණු වැනි පූර්ව සලකුණු සහ “ට්රූමන් සලකුණ” (Truman sign) වැනි මුල් රෝග ලක්ෂණ හඳුනාගෙන ඇත. “ට්රූමන් සලකුණ” යනු, 1998 දී තිරගත වූ ‘The Truman Show’ චිත්රපටයේ ප්රධාන චරිතය, රියැලිටි ටීවී වැඩසටහනක පසුතලයක තමා නොදැනුවත්වම ජීවත් වන බවට දැනුණු ආකාරයටම, අමුතු දෙයක් සිදුවෙමින් පවතින බවට මිනිසුන්ට දැනෙන කරදරකාරී හැඟීමකි. “ඔබට මුල සිටම රෝගය වළක්වා ගත හැකි නම්, සමහර විට වර්ධනය වන සියලුම ආබාධිත තත්ත්වයන් සහ නිදන්ගත ගමන් මග වළක්වා ගත හැකිය.”
භින්නෝන්මාදයට ප්රතිශක්තිකරණ පද්ධතිය කොතෙක් දුරට සම්බන්ධද, සහ රෝගී වූවන්ගේ විවිධ උප කණ්ඩායම් තුළ ස්නායු සම්ප්රේෂකයන් වෙනස් විය හැක්කේ කෙසේද වැනි බොහෝ ප්රශ්න විවෘතව පවතී. පර්යේෂකයන් පරිවෘත්තීය ක්රියාවලියේ අසාමාන්යතා වැනි, භින්නෝන්මාදයට යටින් පැවතිය හැකි වෙනත් වැදගත් යාන්ත්රණයන් ද හඳුනාගෙන ඇත. මූලික පර්යේෂණවලින් පෙනී යන්නේ මේදය අධික සහ කාබෝහයිඩ්රේට් අඩු ආහාර වේලක් වන කීටොජෙනික් (ketogenic) ආහාර වේලක් ගැනීමෙන් මෙම රෝගයේ සමහර රෝග ලක්ෂණ සමනය විය හැකි බවයි. භින්නෝන්මාදයෙන් පෙළෙන අයට ප්රතිකාර කිරීමේදී කථන ප්රතිකාර ද උපකාරී වන බව මතුවෙමින් තිබේ. උදාහරණයක් ලෙස, මිනිසුන්ට ඔවුන්ගේ සිතුවිලි සහ හැසිරීම් රටා සකස් කර ගැනීමට උපකාර කිරීම කෙරෙහි අවධානය යොමු කරන සංජානන-චර්යා ප්රතිකාරය (cognitive-behavioral therapy), මනෝව්යාධියට යටින් පවතින චින්තන රටා නැවත හැඩගැස්වීමට හෝ අඩු අභිප්රේරණයක් හෝ සතුට අත්විඳීමේ හැකියාව අඩුවීම වැනි ඍණාත්මක රෝග ලක්ෂණ සමඟ කටයුතු කිරීමට රෝගීන්ට උපකාර කළ හැකිය.
අවසාන වශයෙන්, බලාපොරොත්තුව වන්නේ භින්නෝන්මාදයෙන් පෙළෙන පුද්ගලයින් සඳහා වඩා හොඳ, වඩා ඉලක්කගත ප්රතිකාර ලබා දීමයි. සමහර වෛද්යවරුන් පවසන්නේ එවැනි සංකීර්ණ රෝග සමඟ කටයුතු කරන්නේ කෙසේද යන්න පිළිබඳ සැලැස්මක් පිළිකා රෝග විද්යා (oncology) ක්ෂේත්රය සතුව ඇති බවයි. වරක් තනි රෝගයක් ලෙස දකිනු ලැබූ පිළිකාව, දැන් තනි නමකින් ඒකාබද්ධ වූ, විවිධ හේතු සහ යාන්ත්රණ සහිත රෝග රාශියක එකතුවක් ලෙස සැලකේ. පිළිකා ප්රතිකාර සඳහා පුද්ගලීකරණය කළ ප්රතිකාර (personalized therapies) වඩ වඩාත් ජනප්රිය වන්නා සේම, පර්යේෂකයන් මෙම ප්රවේශය භින්නෝන්මාදය සහ අනෙකුත් මානසික රෝගවලට ප්රතිකාර කිරීමේ අනාගතය ලෙස දකී.
“නිරවද්ය වෛද්ය විද්යාව (Precision medicine) යනු භින්නෝන්මාද ප්රතිකාරයේ කතාවේ විශාල කොටසක් ලෙස මතු වනු ඇතැයි මා සිතන දෙයක්,” ක්රිස්ටල් පවසයි. අවසානයේදී, වෛද්යවරුන්ට රෝගීන්ට, “ඔබට ඇත්තේ මෙම ජීව විද්යාවයි, ඔබට අවශ්ය එම ප්රතිකාරයයි” කියා පැවසීමට හැකි වනු ඇතැයි ඔහු බලාපොරොත්තු වේ. “භින්නෝන්මාදයේ මෙම ජීව විද්යාව අවබෝධ කර ගැනීමේ අනාගතය අපව රැගෙන යනු ඇතැයි මා සිතන්නේ එතැනටයි.”
ඩයනා ක්වොන් විසිනි (සයන්ටිෆික් ඇමරිකන් සඟරාව)





ප්රතිචාරයක් ලබාදෙන්න